
Veröffentlicht am: 5. Mai 2021
Autoren: Prof. Dr. Burkhard Schütz, MSc ETH Michelle Passarge
Pandemien sind nicht nur ein medizinisches Phänomen; sie betreffen den Einzelnen und die Gesellschaft auf vielen Ebenen. Sie verursachen Störungen. Panik und Stress sind mit Ausbrüchen in Verbindung gebracht worden. In dem Maße, wie die Besorgnis über die wahrgenommene Bedrohung wächst, beginnen die Menschen Mehl, Nudeln, Toilettenpapier oder auch Masken und andere medizinische Hilfsgüter zu horten. Darauf folgen oft angstbezogene Verhaltensweisen, Schlafstörungen und ein insgesamt schlechterer wahrgenommener Gesundheitszustand. Menschen mit psychischen Erkrankungen können besonders anfällig für die Auswirkungen einer weit verbreiteten Panik und Bedrohung sein.
Chronische Krankheiten sind häufig mit psychischen Störungen assoziiert [[1], [2]]. Auch nach Infektionen steigen Depressionsraten stark an [[3], [4]]. Obwohl die Auswirkungen der Coronavirus- Pandemie auf die psychische Gesundheit nicht systematisch untersucht worden sind, wird erwartet, dass COVID-19 nicht zuletzt aufgrund der starken Medienpräsenz über Monate hinweg Folgen haben wird. COVID-19 schürt Angst auf gesellschaftlicher Ebene. Auf individueller Ebene kann sie Angst verschlimmern, zu Stress, Depressionen oder unspezifischen psychischen Problemen führen. Häufig beobachtet werden Stimmungsprobleme, Schlafstörungen und phobie- oder panikähnliche Symptome, die zu einer Zunahme von Hand-, Hautekzemen und Allergien führen [[5], [6]].
Neben gesundheitlichen Problemen als Folge der Pandemie wird auch die stark einbrechende Weltwirtschaft mit steigenden Arbeitslosenzahlen und zahlreichen Firmeninsolvenzen die Gesundheit der Menschen belasten. Eine Studie von Ioannis Laliotis et al. [7] in „The Lancet Public Health“ untersuchte die gesundheitlichen Folgen der Wirtschaftskrise in Griechenland. Neben einer Zunahme der Gesamtmortalität fällt v.a. eine deutlich steigende Selbstmordrate auf. Menschen berichten von höherem Stress aus Angst vor Entlassungen, Gehaltseinbußen oder Veränderungen im Arbeitsumfeld [8]. Angst und geänderte Arbeitsbedingungen führen nicht selten zu Schlaflosigkeit [9], zu Burnout-Symptomen [10] und einem gehäuften Auftreten von Depressionen [11].
Psychischer Stress ist ein wichtiger Faktor für die Entwicklung eines Reizdarmsyndroms (IBS). Hinweise aus klinischen und experimentellen Studien zeigen, dass Stress deutliche Auswirkungen auf die Motilität, Sekretion und Permeabilität des Darms hat. Stressinduzierte Einflüsse wirken auf die Darm-Hirn-Achse und verursachen oft eine Zunahme der Beschwerden [12]. Der Einfluss von Stress in Krisen und die sich daraus ergebenen Belastungen haben nicht nur einen Einfluss bei Patienten mit IBS, sie wirken sich auch auf den Verlauf von chronischer Komplexerkrankungen aus, wie z.B. Morbus Crohn oder Colitis ulcerosa [13].
Befinden wir uns in einer Krise, sei es als Folge der COVID-19 Pandemie oder einer sich daraus ergebenden schweren Finanz- oder Wirtschaftskrise, hat das Folgen für unsere Gesundheit. Haben wir Angst und sind wir gestresst, gerät das sensible Gleichgewicht aus Psyche, Nerven- und Immunsystem durcheinander. Der Mensch wird anfällig für Infektionen, Entzündungen und Allergien. Emotionale Belastung und Stress drücken nicht nur auf das Gemüt, sondern auch auf das Immunsystem [14]. Es kommt zu einer anhaltend vermehrten Freisetzung von Cortisol und Katecholaminen mit Folgen für den Organismus. Stress, Burnout oder oft auch Depressionen gehen mit chronisch subklinischen Entzündungen einher, die zu einer Beeinflussung wichtiger Stoffwechselwege führen [15]. Auch das hat erhebliche Auswirkungen und kann Entstehung und Verlauf von Erkrankungen maßgeblich beeinflussen.
Metabolomanalysen – Neue Wege in eine zukunftsweisende Labordiagnostik
Neben klassischen diagnostischen Ansätzen zum Nachweis von akuten oder chronischen Stressbelastungen auf der Basis von Cortisolbestimmungen im Speichel oder Neurotransmitternachweisen im Urin, gibt es neue Analyseverfahren, sogenannte Metabolomanalysen, die auf einer hoch modernen Technologie beruhen und völlig neue Einblicke in die komplexe Welt der stress- oder angstbedingten Erkrankungen ermöglichen.
Metabolomanalysen berücksichtigen nicht nur Cortisol im Tagesverlauf oder einige Neurotransmitter, sie erfassen die kompletten Stoffwechselwege mit allen wichtigen Metaboliten, Enzymen und Cofaktoren. Dadurch können Störungen viel präziser lokalisiert und Therapieansätze zielgerichteter und effizienter erfolgen.
Metabolomanalysen (s. Abb. 1) stellen neue Ansätze in der Labordiagnostik dar. Sie setzen moderne Untersuchungsverfahren voraus und basieren meist auf einer LC-Tandem-Massenspektrometrie. Es werden nicht wie bisher Einzelparameter analysiert und anschließend zu kleineren Profilen zusammengefasst. Metabolomanalysen ermöglichen eine gleichzeitige Untersuchung von bis zu 70 Metaboliten oder molekularen Analyten, gleichgültig, ob es sich um Aminosäuren, Peptide, Lipide, Zucker oder organische Säuren handelt. Durch gezielte Kombination von enthalten Analyten lassen sich vollständige Stoffwechselwege abbilden. Ausgehend von z.B. Aminosäuren, können alle daraus entstehenden biologisch aktiven Metaboliten berücksichtigt werden, die an der Regulierung von Immunreaktionen, neuronalen Funktionen oder Entzündungsprozessen beteiligt sind. Durch quantitative Erfassung von abhängigen Metaboliten lassen sich Enzymaktivitäten oder Einflüsse von wichtigen Cofaktoren ableiten. Auf Basis von drei oder vier gemessenen Metaboliten muss nicht wie früher über Folgen spekuliert werden. Mit Hilfe der Metabolomanalysen werden Endprodukte der relevanten Stoffwechselwege als Analyten miterfasst, sodass an die Stelle von Vermutungen Fakten treten.
Trotz moderner Messverfahren führen neue diagnostische Ansätze nicht immer zu höheren Preisen: Mit der neuen Metabolomdiagnostik sind Profile, die aus 30 oder mehr Analyten bestehen, deutlich preiswerter zu erbringen als mit konventionellen Einzeluntersuchungen.

Abbildung 1:
Metabolomanalysen: Komplexe Stoffwechselanalysen anstelle von Einzelparameteruntersuchungen.
Beispiel einer Metabolomuntersuchung im Urin über Massenspektrometrie: Mehr als über 70 organische Verbindungen lassen sich identifizieren. (Quelle: Wishart DS. Physiol Rev. 2019;99(4):1819-1875. doi:10.1152/physrev.00035.2018)
Metabolomprofile
Die umfangreichen Metabolomprofile eignen sich im Besonderen für Patienten mit chronischer Stressbelastung, Burnout-Symptomatik, CFS oder auch für depressive Patienten. Es beinhaltet nicht nur die Untersuchung von Katecholaminen und Neurotransmittern, es bietet darüber hinaus einen kompletten Einblick in den Tryptophanstoffwechsel, mit allen wichtigen Metaboliten und Enzymaktivitäten, sowie eine umfangreiche Analyse vieler wichtiger Faktoren, die direkt oder indirekt Einfluss auf die ablaufenden Stoffwechselprozesse nehmen. Enthalten sind folgende Parameter (siehe Abbildung 2):
- Tryptophan-Stoffwechsel: Tryptophan
- Serotonin-Pathway: Serotonin
- Kynurenin-Pathway: L-Kynurenin
Kynureninsäure
3-OH-Kynurenin
Quinolinsäure
NAD (Nicotinamid-Adenin-Dinukleotid)
- Relevante Enzyme: IDO (Indolamin-2,3-Dioxigenase)
KAT (Kynurenin-Oxoglutarat-Transaminase)
KMO (Kynurenin-Monooxigenase)
- Immunaktivierung: Neopterin (Aktivierung durch proinflammatorische Zytokine)
- Katecholamin-Stoffwechsel: Tyrosin
Phenylalanin
Dopamin
Noradrenalin
Adrenalin
- Weitere Neurotransmitter: GABA
Glutamat
- Wichtige Cofaktoren: Vitamin B6 (Cystathionin)
Vitamin B12 (Methylmalonsäure)
Vitamin B3 (Nicotinsäure, NAD, Nicotinamid)
Tetrahydrobiopterin (BH4)
- Methylgruppen-Donatoren: SAM
(Methylierungsaktivität) Betain
Cholin
- NO-Stress/Mitochondrien: Citrullin
Methylmalonsäure
Suberinsäure
Citrat
Laktat/Pyruvat
- Fettsäureverbrennung: L-Carnitin
- Entzündung/Arteriosklerose: TMAO, TMA

Abbildung 2:
Zusammenhang zwischen dem Tryptophan- und Katecholaminmetabolismus sowie weiteren Stoffwechselprozessen. Die Graphik veranschaulicht die im Metabolomprofil enthaltenen Parameter. (Quelle: eigene Abbildung)
Metabolomuntersuchungen ermöglichen einen zeitgleichen Einblick in alle relevanten Ebenen des Stoffwechsels. Sie ermöglichen viel besser eine Klärung von ursächlichen Faktoren, als das über Einzelparameteranalysen oder Stufenkonzepte je möglich wäre.
Tryptophanstoffwechsel
Der Tryptophanstoffwechsel hat eine zentrale Bedeutung für die Gesundheit des Menschen. Er reguliert wichtige neurochemische Funktionen und Teile des Immunsystems [16]. Verschiebungen innerhalb des Tryptophanstoffwechsels durch Angst, Stress oder dadurch hervorgerufene subklinische Entzündungsreaktionen können negative Einflüsse auf Krankheitsverläufe und Heilungschancen haben.
Tryptophan (TRP) ist seit Langem als Vorläufer von Serotonin bekannt. Doch unter normalen Umständen werden kaum mehr als 2 – 4 % von TRP in Serotonin umgewandelt. Der weitaus größte Teil wird dem Kynurenin-Stoffwechselweg zugeführt. Es entsteht L- Kynurenin (KYN), ein Metabolit, der v.a. in der Leber weiter zu 3-OH-Kynurenin und Quinolinsäure umgewandelt wird [17]. Aus Quinolinsäure entsteht NAD, das gebraucht wird für eine effektive Energiegewinnung in den Mitochondrien. Mehr als 90 % des Tryptophans werden in NAD umgewandelt, etwa 4 % auch in Kynureninsäure, ein ebenfalls wichtiger Metabolit, der antientzündlich wirkt, vor oxidativem Stress schützt und v.a. auch neuroprotektive Eigenschaften aufweist [18].
Serotonin ist ein wichtiger inhibitorisch wirkender Neurotransmitter und Vorläufer des Schlafhormons Melatonin. Zur Produktion von Serotonin ist der Körper auf eine ausreichende Versorgung mit Tryptophan angewiesen, das in eiweißhaltiger Nahrung vorkommt [19]. Wichtige Cofaktoren für die Serotoninsynthese sind Vitamine des B-Komplexes, v.a. Vitamin B6 und Folsäure. Einen Einfluss hat auch Niacin. Serotonin wirkt Stress entgegen, reguliert den Blutdruck, die Darmbewegung, wirkt entspannend, stimmungsaufhellend, schlafregulierend, angstlösend, antidepressiv und hat einen positiven Einfluss auf viele Gehirnleistungen [[20], [21]].
Folgen von Angst und anhaltenden Belastungen für Tryptophanmetabolismus und Menschen
Der TRP-Stoffwechsel kann die Physiologie des Körpers auf verschiedenen Ebenen beeinflussen und tief in funktionelle Prozesse eingreifen. Störungen und Dysbalancen sind mit zahlreichen Erkrankungen assoziiert. Eine entsprechende Regulierung ist daher Grundlage für effektive Therapieansätze.
Angst führt zu Stress und der ist Ursache für eine vermehrte Freisetzung von inflammatorischen Zytokinen (z.B. IFN-α, -ß, -γ, TNF-α, IL-6), die über Enzymaktivierungen in Immunzellen eine erhebliche Beeinflussung des Tryptophanstoffwechsels hervorrufen [22]. Aktiviert werden dabei v.a. die Enzyme IDO und KMO, wodurch wesentlich mehr TRP über den KYN-Pfad abgebaut wird und folglich nicht mehr für die Serotoninsynthese zur Verfügung steht. Es kommt zu einer vermehrten Produktion von Quinolinsäure, die, anders als in der Leber, in Immunzellen nicht weiter in NAD umgewandelt werden kann. Sie reichert sich im Kreislauf an und wird über die Nieren ausgeschieden [23]. Ansteigende Quinolinsäurespiegel wirken sich negativ aus, denn Quinolinsäure wirkt neurotoxisch, entzündungsfördernd und prooxidativ [24]. Durch Anreicherung von Quinolinsäure werden neuronale Störungen begünstigt und die Blut-Hirn-Schranke geschädigt. Da Quinolinsäure in Immunzellen aber nicht in NAD umgewandelt werden kann, sinken die NAD-Mengen dramatisch, um mehr als 90 %. Dies bleibt für die Mitochondrien nicht folgenlos. Es fehlt ein wichtiger Cofaktor und damit letztlich Energie!
Stress ausgelöst durch Belastungssituationen kann somit über den TRP-Stoffwechsel psychische Erkrankungen hervorrufen [25]. Auch eine schwere Depression kann mit Verschiebungen im TRP-Stoffwechsel assoziiert sein [26]. Ein Ungleichgewicht von neurotoxischen und neuroprotektiven Kynurenin-Metaboliten ist charakteristisch für solche Fälle [27]. So werden bei Patienten mit schweren Depressionen oft erhöhte Konzentrationen an Kynurenin, 3-OH-Kynurenin und Quinolinsäure gefunden, sowie erniedrigte Kynureninsäure- und vor allem niedrige NAD-Spiegel. Es ist nicht verwunderlich, dass aufgrund des NAD-Mangels oft eine deutliche Beeinträchtigung der Zellatmung beobachtet wird [28]. Mitochondrien-Untersuchungen, wie der bioenergetische Gesundheitsindex, zeigen eine abfallende Maximalatmung. Es ist also nicht mehr möglich durch Steigerung der Zellatmung eine wachsende Energieanforderung zu kompensieren. Betroffene werden kraft- und energielos.
Durch die entzündungsbedingte Verschiebung im Tryptophanstoffwechsel fehlt es nicht nur an NAD, es wird auch deutlich weniger Tryptophan in Serotonin und Kynureninsäure umgewandelt, ihre Menge geht um 50 – 70 % zurück, mit negativen Folgen für den Betroffenen [29]. Ein Abfall der Serotoninbildung im ZNS wirkt sich negativ auf die Stimmung der Menschen aus. Beeinträchtigungen des Gefühlslebens, bis hin zu Depressionen können die Folge sein [30]. Auch die Lern- und Konzentrationsfähigkeit nimmt ab [20]. Da mit sinkenden Serotoninspiegeln auch weniger Melatonin gebildet wird, sind Schlafstörungen die Folge [31]. Der Schlaf-Wach-Rhythmus wird mehr und mehr gestört, mit allen sich daraus ergebenden Konsequenzen.
Serotonin und Kynureninsäure sind auch von eminenter Bedeutung für die Steuerung von Darmfunktionen [21]. Angst- und stressinduzierte Veränderungen im TRP-Stoffwechsel gehen daher regelmäßig mit einer deutlichen Zunahme von Reizdarmsyndromen einher, geprägt durch Diarrhö, Obstipation oder einer begleitenden Schmerzsymptomatik [[32], [33]].
Um diese vielfältigen Beschwerden erfolgreich behandeln zu können, muss man ihre Ursachen kennen. Dazu braucht es einen umfangreichen Einblick in den gesamten Tryptophanmetabolismus und damit assoziierte Stoffwechselsysteme.
Katecholamine und Aminosäuren
Die essentielle Aminosäure Phenylalanin ist Ausgangspunkt der Katecholaminsynthese. Unter Einfluss der Cofaktoren Tetrahydrobiopterin (BH4) und Eisen wird Phenylalanin durch Hydroxylierung in Tyrosin umgewandelt, das weiter über L-DOPA in Dopamin metabolisiert wird (s. Abb. 3). Hieraus wird ersichtlich, dass für die Bildung der Katecholamine auch die Aminosäure Tyrosin verwendet werden kann. Phenylalanin ist damit teilweise, aber nicht vollständig durch Tyrosin ersetzbar.
Die Katecholamine Adrenalin, Noradrenalin und Dopamin, die Pulsfrequenz, Herzminutenvolumen und Blutdruck regulieren, werden binnen Sekunden nach einem Stressereignis freigesetzt und, anders als Cortisol, vom Körper sehr schnell wieder abgebaut. Ihre Halbwertszeit liegt nur bei wenigen Minuten. Unter Stress sind die Katecholaminspiegel oft erhöht [34]. Ist der Patient jedoch einer lang andauernden massiven Stresseinwirkung ausgesetzt, leidet er bereits an einem Burnout-Syndrom oder an einem CFS, dann liegen die Messergebnisse oft unterhalb der Norm. Die Produktion an Botenstoffen in Nebenniere und Neuronen hat sich über die lange Stressdauer erschöpft.
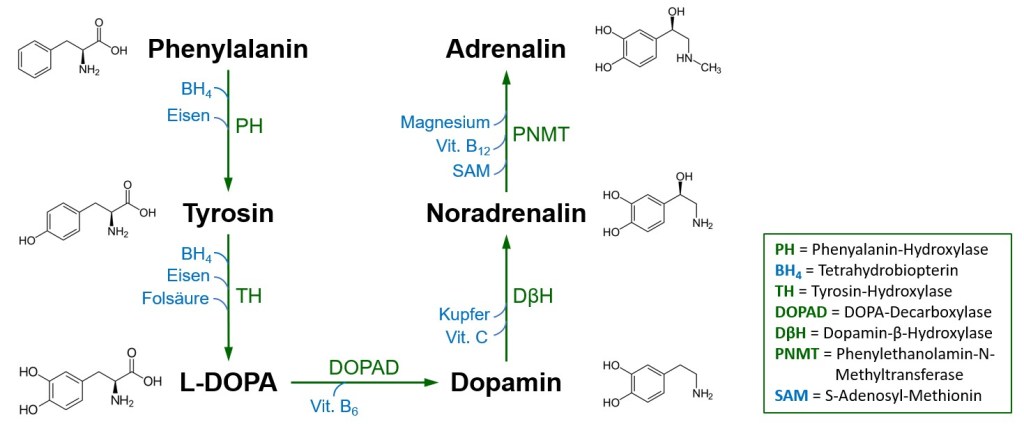
Abbildung 3:
Katecholaminmetabolismus mit relevanten Cofaktoren. (Quelle: eigene Abbildung)
Neurotransmitter
Die Konzentrationen der Neurotransmitter Glutamat und GABA liegen etwa 1000-fach höher als die Konzentrationen von Noradrenalin oder Dopamin. Glutamat wirkt u.a. fördernd auf Motorik, Lernen und Gedächtnis [35]. GABA stabilisiert den Blutdruck, reguliert den Appetit, wirkt angstlösend und schlaffördernd.
Wichtige Cofaktoren
Vitamin B6 ist ein wichtiger Cofaktor im Rahmen der Neurotransmittersynthese und des TRPStoffwechsels. Fehlt das Vitamin, kann L-DOPA nicht in Dopamin und Noradrenalin nicht in Adrenalin umgewandelt werden. Im Tryptophanstoffwechsel benötigen die Metabolisierungsschritte von 5-HTP zu Serotonin, von Kynurenin zu Kynureninsäure und von 3-OH-Kynurenin zu Quinolinsäure Vitamin B6 als Cofaktor [36]. Im Profil enthalten ist nicht Vitamin B6 sondern Cystathionin, ein funktioneller Marker für die Versorgung mit bioaktivem Vitamin B6 [37].
Vitamin B12 ist ein Cofaktor der Methyltransferase, die für die Umwandlung von Noradrenalin in Adrenalin verantwortlich ist. Auch Vitamin B12 wird nicht direkt gemessen, sondern Methylmalonsäure, einer der sensibelsten Marker für einen präklinischen Vitamin B12-Mangel [38].
Vitamin B3 hat Einfluss auf den Kynurenin-Stoffwechselweg. Eine gute Versorgung mit Niacin führt zu einer Herunterregulierung der Kynureninsynthese [39]. Im Profil enthalten ist aber nicht nur die Bestimmung von Niacin, sondern auch von Nicotinamid und NAD. Nicotinamid wird vor allem über die Nahrung zugeführt. Das aus Quinolinsäure gebildete NAD hingegen stammt aus dem TRP-Metabolismus und ist unabdingbar für eine ausreichende ATP-Produktion in den Mitochondrien [28].
Tetrahydrobiopterin (BH4) ist ein wichtiger Cofaktor im menschlichen Stoffwechsel. Die wichtigsten Reaktionen, bei denen BH4 als Cofaktor auftritt, sind in Abbildung 4 wiedergegeben. Die Stoffwechselreaktionen beinhalten Katecholamin– und Serotoninsynthese, sowie die Umwandlung von Arginin in Stickstoffmonoxid (NO) und Citrullin. Fehlt BH4 hemmt das die ablaufenden enzymatischen Prozesse.
- Umbau von Phenylalanin è Tyrosin (Enzym: Phenylalanin-Hydroxylase)
- Umwandlung von Tyrosin è L-DOPA (Enzym: Tyrosin-Hydroxylase)
- Umwandlung von Arginin è NO + Citrullin (Enzym: NO-Synthase)
- Oxidation von Tryptophan è 5-HTP (Enzym: Tryptophan-Hydroxylase)

Abbildung 4:
Tetrahydrobiopterin (BH4) als Cofaktor wichtiger Stoffwechselwege, wie Serotonin-, Dopamin- und NO-Synthese.
GTP-CH1: Guanosintriphosphat-Cyclohydrolase-1; BH4: Tetrahydrobiopterin; BH2: Biopterin. (Quelle: modifiziert nach [40])
Methylgruppendonatoren
Unter Methylierung versteht man die Übertragung von Methylgruppen innerhalb einer chemischen Reaktion von einem Molekül auf ein anderes. S-Adenosylmethionin (SAM) stellt einen der wichtigsten Methylgruppendonatoren bei Entgiftungs- und Synthesereaktionen dar [41]. So stammen z.B. die Methylgruppen des Adrenalins hauptsächlich von SAM. Andere wichtige Methylgruppendonatoren sind Betain und Cholin. Sind Methylgruppendonatoren nicht in ausreichender Menge vorhanden, hat das Folgen für die Adrenalinsynthese und die Spiegel sinken.
Methylierungen betreffen auch DNA, RNA, Proteine und Lipide. DNA-Methylierungen haben bedeutende biologische Funktionen. Sie tragen zur Entgiftung von Homocystein oder Histamin bei, sind Teil des epigenetischen Codes und stellen den wichtigsten Einflussfaktor für epigenetische Veränderungen dar (s. Abb. 5) [42].

Abbildung 5:
Methylierungszyklus und seine Anbindung an Folsäure-, BH4 und Harnstoffzyklus.
NO-Stress und mitochondriale Funktionsmarker
Entzündungen ausgelöst durch Angst oder chronischen Stress beeinflussen über eine Fehlleitung des TRP-Stoffwechsels und BH4-Zyklus die Serotonin- und Katecholaminsynthese [21]. Aus einem erhöhten Verbrauch von Neurotransmittern durch Stress und einer gestörte Neusynthese resultiert eine zunehmende Depletion der Neuronen. Der Mensch fühlt sich ausgebrannt, müde und kraftlos.
Will man den Einfluss von chronischem Stress und einer daraus entstehenden Silent Inflammation auf die Gesundheit des Menschen verstehen und gezielte Maßnahmen ergreifen, um den Patienten zu helfen, reicht es nicht, den Katecholamin- und Tryptophanstoffwechsel zu untersuchen, es müssen auch erste mitochondriale Marker mit einbezogen werden, die eine ergänzende Aussage zur Mitochondrienfunktion ermöglichen. Auch diese sind in der Metabolomanalyse enthalten.
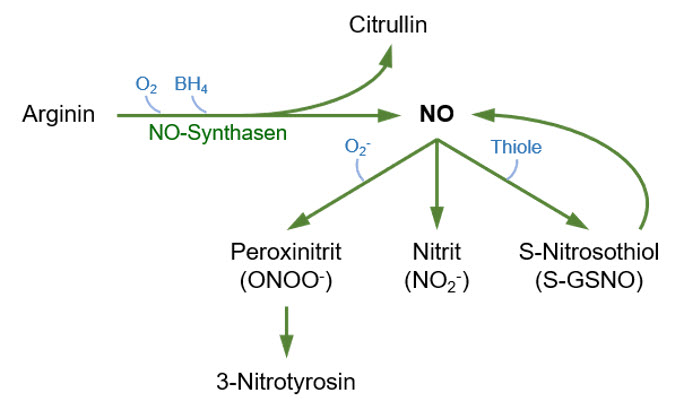
Abbildung 6:
Umwandlung von Arginin und O2 über NO-Synthasen in Stickstoffmonoxid (NO) und Citrullin. Weitere Metabolisierung in u.a. Peroxinitrit und 3-Nitrotyrosin. (Quelle: eigene Abbildung)
Citrullin und Citrat lassen Rückschlüsse auf nitrosativen Stress zu. Ein Anstieg von Citrullin spricht für eine erhöhte NO-Synthese aus Arginin (s. Abb. 6), steigende Citrat-Werte hingegen lassen auf eine mitochondriale Fehlfunktion schließen. Durch die Affinität von NO zu Fe-haltigen Enzymen wird die Aconitase im Zitratzyklus gehemmt. Der weitere Umbau von Citrat zu Isocitrat ist damit gestört. Methylmalonsäure ist ein funktioneller Marker für einen Mangel an Vitamin B12, das als NO-Gegenspieler imstande ist, die Blockade Fe-haltiger Enzyme durch NO zu lösen [38].
Auch die im Profil enthaltenen organischen Säuren Laktat und Pyruvat lassen mitochondriale Störungen erkennen. Kommt es durch Ernährungsfaktoren zusätzlich zu einem Mangel an L-Carnitin, können langkettige Fettsäuren aus der ß-Oxidation nicht mehr der mitochondrialen Energiegewinnung zugeführt werden [43]. L-Carnitin versorgt die Mitochondrien mit Brennstoffen, indem es Fettsäuren vom Cytosol in die Mitochondrien transportiert. Ein Mangel an L-Carnitin kann also Energiedefizite und damit verbundene Symptome verstärken [44]. Bei einer Störung der ß-Oxidation oder fehlendem L-Carnitin werden Fettsäuren alternativ durch w-Oxidation zu mittelkettigen Dicarbonsäuren abgebaut, die im Urin ausgeschieden werden. Hierzu gehört z.B. die Suberinsäure. Ein Anstieg dieses Markers im Profil weist also auf o.g. Störungen hin [45].
TMAO (Trimethylamin-N-Oxid)
Bestimmte Darmbakterien sind imstande Cholin, Betain oder L-Carnitin so zu metabolisieren, dass daraus TMA (Trimethylamin) entsteht, das in der Leber weiter zu TMAO abgebaut wird (s. Abb. 7) [[46], [47]]. TMAO wird mit Entzündungen, Arteriosklerose und im weiteren Sinne mit kardiovaskulären Erkrankungen in Verbindung gebracht [[48], [49]]. Mit in das Profil aufgenommen wurde TMAO vor allem wegen seiner entzündungsfördernden Eigenschaften, die über eine vermehrte Freisetzung proinflammatorischer Zytokine den Tryptophanstoffwechsel beeinflussen. Serotonin- und NAD-Synthese werden gehemmt. Gleichzeitig wird über eine Beeinträchtigung des BH4-Zyklus auch die Katecholaminbildung gestört. Eine angst- und stressinduzierte subklinische Entzündung kann durch begleitende Faktoren verstärkt werden. Veränderungen des Darmmikrobioms stellen hierbei einen wichtigen und vor allem häufigen Faktor dar.

Abbildung 7:
Bildung von TMAO. Cholin, Betain und L-Carnitin aus verschiedenen Nahrungsmitteln werden im Darm enzymatisch durch einige Bakterien zu TMA und in der Leber weiter zu TMAO umgewandelt. TMAO wird in Zusammenhang mit Entzündungen, Arteriosklerose / kardiovaskulären Erkrankungen gebracht. (Quelle: modifiziert nach M. H. Janeiro et al., 2018 [50])
Literaturangaben:
[1] L. Van Den Heuvel et al., “Frequency and correlates of anxiety and mood disorders among TB- and HIV-infected Zambians,” AIDS Care – Psychol. Socio-Medical Asp. AIDS/HIV, vol. 25, no. 12, pp. 1527–1535, May 2013, doi: 10.1080/09540121.2013.793263.
[2] V. Kuan et al., “A chronological map of 308 physical and mental health conditions from 4 million individuals in the English National Health Service,” Artic. Lancet Digit. Heal., vol. 1, pp. 63–77, 2019, doi: 10.1016/S2589-7500(19)30012-3.
[3] S. D. Gale, A. N. Berrett, L. D. Erickson, B. L. Brown, and D. W. Hedges, “Association between virus exposure and depression in US adults,” Psychiatry Res., vol. 261, pp. 73–79, Mar. 2018, doi: 10.1016/j.psychres.2017.12.037.
[4] B. W. Mason, “Acute psychological effects of suspected bioterrorism,” J Epidemiol Community Heal., vol. 57, pp. 353–354, 2003, doi: 10.1136/jech.57.5.353.
[5] M. A. Gupta and A. K. Gupta, “Self-induced dermatoses: A great imitator,” Clin. Dermatol., vol. 37, no. 3, pp. 268–277, May 2019, doi: 10.1016/j.clindermatol.2019.01.006.
[6] U. Gieler et al., “Self-inflicted lesions in dermatology: Terminology and classification – A position paper from the European Society for dermatology and psychiatry (ESDaP),” Acta Derm. Venereol., vol. 93, no. 1, pp. 4–12, 2013, doi: 10.2340/00015555-1506.
[7] I. Laliotis, J. P. A. Ioannidis, and C. Stavropoulou, “Total and cause-specific mortality before and after the onset of the Greek economic crisis: an interrupted time-series analysis,” Lancet Public Heal., vol. 1, no. 2, pp. e56–e65, Dec. 2016, doi: 10.1016/S2468-2667(16)30018-4.
[8] F. J. Tsai and C. C. Chan, “The impact of the 2008 financial crisis on psychological work stress among financial workers and lawyers,” Int. Arch. Occup. Environ. Health, vol. 84, no. 4, pp. 445–452, Apr. 2011, doi: 10.1007/s00420-010-0609-0.
[9] E. Nena, P. Steiropoulos, N. Papanas, D. Kougkas, P. Zarogoulidis, and T. Constantinidis, “Greek financial crisis: From loss of money to loss of sleep?,” Hippokratia, vol. 18, no. 2, p. 135, 2014.
[10] J. Wray, “The impact of the financial crisis on nurses and nursing,” J. Adv. Nurs., vol. 69, no. 3, pp. 497–499, Mar. 2013, doi: 10.1111/jan.12031.
[11] A. Belke, “Depression and grief as a result of economic and financial crises: the example of Greece and some generalizations,” Econ. Chang. Restruct., vol. 53, no. 1, pp. 139–149, Feb. 2020, doi: 10.1007/s10644-019-09249-5.
[12] H. Y. Qin, C. W. Cheng, X. D. Tang, and Z. X. Bian, “Impact of psychological stress on irritable bowel syndrome,” World J. Gastroenterol., vol. 20, no. 39, pp. 14126–14131, Oct. 2014, doi: 10.3748/wjg.v20.i39.14126.
[13] E. M. Szigethy et al., “White Paper AGA: The Impact of Mental and Psychosocial Factors on the Care of Patients With Inflammatory Bowel Disease,” Clin. Gastroenterol. Hepatol., vol. 15, no. 7, pp. 986–997, Jul. 2017, doi: 10.1016/j.cgh.2017.02.037.
[14] J. N. Morey, I. A. Boggero, A. B. Scott, and S. C. Segerstrom, “Current directions in stress and human immune function,” Curr. Opin. Psychol., vol. 5, pp. 13–17, Oct. 2015, doi: 10.1016/j.copsyc.2015.03.007.
[15] R. Dantzer, J. C. O’Connor, G. G. Freund, R. W. Johnson, and K. W. Kelley, “From inflammation to sickness and depression: When the immune system subjugates the brain,” Nat. Rev. Neurosci., vol. 9, no. 1, pp. 46–56, Jan. 2008, doi: 10.1038/nrn2297.
[16] R. Schwarcz and T. W. Stone, “The kynurenine pathway and the brain: Challenges, controversies and promises,” Neuropharmacology, vol. 112, pp. 237–247, Jan. 2017, doi: 10.1016/j.neuropharm.2016.08.003.
[17] L. Palego, L. Betti, A. Rossi, and G. Giannaccini, “Tryptophan Biochemistry: Structural, Nutritional, Metabolic, and Medical Aspects in Humans,” J. Amino Acids, vol. 2016, pp. 1–13, Jan. 2016, doi: 10.1155/2016/8952520.
[18] Y. Chen and G. J. Guillemin, “Kynurenine Pathway Metabolites in Humans: Disease and Healthy States,” Int. J. Tryptophan Res., vol. 2, p. 1, 2009.
[19] N. Le Floc’h, W. Otten, and E. Merlot, “Tryptophan metabolism, from nutrition to potential therapeutic applications,” Amino Acids, vol. 41, no. 5, pp. 1195–1205, Nov. 2010, doi: 10.1007/s00726-010-0752-7.
[20] D. Š. Štrac, N. Pivac, and D. Mück-Šeler, “The serotonergic system and cognitive function,” Transl. Neurosci., vol. 7, no. 1, pp. 35–49, Jan. 2016, doi: 10.1515/tnsci-2016-0007.
[21] J. M. Gostner, S. Geisler, M. Stonig, L. Mair, B. Sperner-Unterweger, and D. Fuchs, “Tryptophan Metabolism and Related Pathways in Psychoneuroimmunology: The Impact of Nutrition and Lifestyle,” Neuropsychobiology, pp. 1–11, Feb. 2019, doi: 10.1159/000496293.
[22] I. Cervenka, L. Z. Agudelo, and J. L. Ruas, “Kynurenines: Tryptophan’s metabolites in exercise, inflammation, and mental health,” Science (80-. )., vol. 357, no. 6349, Jul. 2017, doi: 10.1126/science.aaf9794.
[23] G. J. Guillemin, “Quinolinic acid, the inescapable neurotoxin,” FEBS J., vol. 279, no. 8, pp. 1356–1365, Apr. 2012, doi: 10.1111/j.1742-4658.2012.08485.x.
[24] V. P.-D. La Cruz, P. Carrillo-Mora, and A. Santamaria, “Quinolinic Acid, an Endogenous Molecule Combining Excitotoxicity, Oxidative Stress and Other Toxic Mechanisms,” Int. J. Tryptophan Res., vol. 5, p. IJTR.S8158, Jan. 2012, doi: 10.4137/IJTR.S8158.
[25] E. Höglund, O. Overli, and S. Winberg, “Tryptophan Metabolic Pathways and Brain Serotonergic Activity: A Comparative Review,” Front. Endocrinol. (Lausanne)., vol. 10, p. 158, Apr. 2019, doi: 10.3389/fendo.2019.00158.
[26] M. Wichers and M. Maes, “The role of indoleamine 2,3-dioxygenase (IDO) in the pathophysiology of interferon-a-induced depression,” J. Psychiatry Neurosci., vol. 29, no. 1, pp. 11–17, Jan. 2004.
[27] E. Won and Y.-K. Kim, “Stress, the Autonomic Nervous System, and the Immune-kynurenine Pathway in the Etiology of Depression,” Curr. Neuropharmacol., vol. 14, no. 7, pp. 665–673, Sep. 2016, doi: 10.2174/1570159×14666151208113006.
[28] L. R. Stein and S. I. Imai, “The dynamic regulation of NAD metabolism in mitochondria,” Trends Endocrinol. Metab., vol. 23, no. 9, pp. 420–428, Sep. 2012, doi: 10.1016/j.tem.2012.06.005.
[29] Q. Wang, D. Liu, P. Song, and M.-H. Zou, “Tryptophan-kynurenine pathway is dysregulated in inflammation, and immune activation.,” Front. Biosci. (Landmark Ed., vol. 20, pp. 1116–43, Jun. 2015.
[30] A.-M. Myint, “Kynurenines: From the perspective of major psychiatric disorders,” FEBS J., vol. 279, no. 8, pp. 1375–1385, Apr. 2012, doi: 10.1111/j.1742-4658.2012.08551.x.
[31] R. Hardeland, “Neurobiology, Pathophysiology, and Treatment of Melatonin Deficiency and Dysfunction,” Sci. World J., vol. 2012, 2012, doi: 10.1100/2012/640389.
[32] T. O. C. Kilkens, A. Honig, M. A. Van Nieuwenhoven, W. J. Riedel, and R. J. M. Brummer, “Acute tryptophan depletion affects brain-gut responses in irritable bowel syndrome patients and controls,” Gut, vol. 53, no. 12, pp. 1794–1800, Dec. 2004, doi: 10.1136/gut.2004.041657.
[33] P. Fitzgerald et al., “Tryptophan catabolism in females with irritable bowel syndrome: relationship to interferon-gamma, severity of symptoms and psychiatric co-morbidity,” Neurogastroenterol. Motil., vol. 20, no. 12, pp. 1291–1297, Dec. 2008, doi: 10.1111/j.1365-2982.2008.01195.x.
[34] D. J. Lodge and A. A. Grace, “Developmental pathology, dopamine, stress and schizophrenia,” Int. J. Dev. Neurosci., vol. 29, no. 3, pp. 207–213, May 2011, doi: 10.1016/j.ijdevneu.2010.08.002.
[35] G. Daoudal and D. Debanne, “Long-Term Plasticity of Intrinsic Excitability: Learning Rules and Mechanisms,” Learn. Mem., vol. 10, no. 6, pp. 456–465, Nov. 2003, doi: 10.1101/lm.64103.
[36] M. Majewski, A. Kozłowska, E. Lepiarczyk, and W. Grzegorzewski, “Overview of the role of vitamins and minerals on the kynurenine pathway in health and diseases,” Artic. J. Physiol. Pharmacol. an Off. J. Polish Physiol. Soc., 2016.
[37] S. Singh, P. Madzelan, and R. Banerjee, “Properties of an unusual heme cofactor in PLP-dependent cystathionine β-synthase,” Nat. Prod. Rep., vol. 24, no. 3, pp. 631–639, May 2007, doi: 10.1039/b604182p.
[38] P. Vashi, P. Edwin, B. Popiel, C. Lammersfeld, and D. Gupta, “Methylmalonic acid and homocysteine as indicators of Vitamin B-12 deficiency in cancer,” PLoS One, vol. 11, no. 1, Jan. 2016, doi: 10.1371/journal.pone.0147843.
[39] A. A.-B. Badawy, “Tryptophan Metabolism: A Versatile Area Providing Multiple Targets for Pharmacological Intervention,” Egypt. J. Basic Clin. Pharmacol., vol. 9, 2019, doi: 10.32527/2019/101415.
[40] N. Castanon, G. Luheshi, and S. Layé, “Role of neuroinflammation in the emotional and cognitive alterations displayed by animal models of obesity,” Front. Neurosci., vol. 9, no. JUL, p. 229, Jul. 2015, doi: 10.3389/fnins.2015.00229.
[41] S. Grégoire et al., “Therapeutic benefits of the methyl donor S-adenosylmethionine on nerve injury-induced mechanical hypersensitivity and cognitive impairment in mice,” Pain, vol. 158, no. 5, pp. 802–810, May 2017, doi: 10.1097/j.pain.0000000000000811.
[42] M. Szyf, “Epigenetics, DNA Methylation, and Chromatin Modifying Drugs,” Annu. Rev. Pharmacol. Toxicol., vol. 49, no. 1, pp. 243–263, Feb. 2009, doi: 10.1146/annurev-pharmtox-061008-103102.
[43] N. Longo, M. Frigeni, and M. Pasquali, “Carnitine transport and fatty acid oxidation,” Biochim. Biophys. Acta – Mol. Cell Res., vol. 1863, no. 10, pp. 2422–2435, Oct. 2016, doi: 10.1016/j.bbamcr.2016.01.023.
[44] E. Arrigoni-Martelli and V. Caso, “Carnitine protects mitochondria and removes toxic acyls from xenobiotics.,” Drugs Exp. Clin. Res., vol. 27, no. 1, pp. 27–49, Jan. 2001.
[45] M. S. de Moraes et al., “Oxidative damage in mitochondrial fatty acids oxidation disorders patients and the in vitro effect of l-carnitine on DNA damage induced by the accumulated metabolites,” Arch. Biochem. Biophys., vol. 679, p. 108206, Jan. 2020, doi: 10.1016/j.abb.2019.108206.
[46] R. A. Koeth et al., “Intestinal microbiota metabolism of l-carnitine, a nutrient in red meat, promotes atherosclerosis,” Nat. Med., vol. 19, no. 5, pp. 576–585, May 2013, doi: 10.1038/nm.3145.
[47] D. Fennema, I. R. Phillips, and E. A. Shephard, “Trimethylamine and trimethylamine N-oxide, a Flavin-Containing Monooxygenase 3 (FMO3)-mediated host-microbiome metabolic axis implicated in health and disease,” Drug Metab. Dispos., vol. 44, no. 11, pp. 1839–1850, 2016, doi: 10.1124/dmd.116.070615.
[48] S. Subramaniam and C. Fletcher, “Trimethylamine N-oxide: breathe new life,” Br. J. Pharmacol., vol. 175, no. 8, pp. 1344–1353, Apr. 2018, doi: 10.1111/bph.13959.
[49] M. T. Velasquez, A. Ramezani, A. Manal, and D. S. Raj, “Trimethylamine N-oxide: The good, the bad and the unknown,” Toxins (Basel)., vol. 8, no. 11, Nov. 2016, doi: 10.3390/toxins8110326.
[50] M. H. Janeiro, M. J. Ramírez, F. I. Milagro, J. A. Martínez, and M. Solas, “Implication of trimethylamine n-oxide (TMAO) in disease: Potential biomarker or new therapeutic target,” Nutrients, vol. 10, no. 10, Oct. 2018, doi: 10.3390/nu10101398.
